Souvent associée aux centrales nucléaires ou aux catastrophes, la radioactivité est avant tout un phénomène physique naturel. Elle se définit par la désintégration spontanée de noyaux atomiques instables, qui émettent des particules et de l’énergie. Mais au-delà de la théorie, elle a des applications très concrètes : en médecine pour traiter certains cancers, en archéologie pour dater des vestiges ou encore dans la production d’électricité. Comprendre la radioactivité, c’est donc mieux saisir un concept clé du programme… et ses enjeux dans le monde réel.
Qu’est-ce qu’un noyau ?
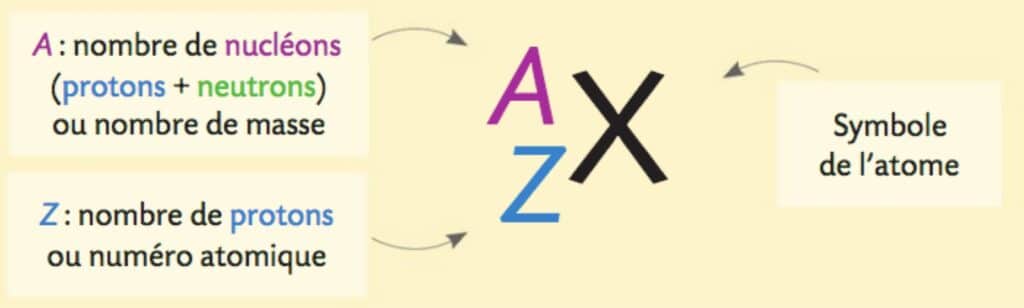
Le noyau est constitué de nucléons ( protons + neutrons ) :
- Le proton possède une charge élémentaire (e = 1,602.10^(-19) C)
- Le neutron ne possède pas de charge élémentaire.
Le noyau est donc chargé positivement.
La masse d’un proton ( mp = 1,6726.10^(-27) kg) est à peu près égale à celle d’un neutron (mn = 1,6749.10^(-27) kg) mais elles sont nettement supérieures à celle d’un électron (me = 9,1090^(-27) kg). C’est pourquoi le noyau concentre quasiment toute la masse de l’atome.
Force nucléaire
Dans un noyau, quatre forces sont en équilibre : la force électrostatique, la force d’attraction gravitationnelle, des interactions fortes et des interactions faibles. La force nucléaire est une interaction forte qui maintient les nucléons dans le noyau. Lorsqu’un noyau est radioactif, le noyau est instable, c’est parce que la force électrostatique (répulsion) est supérieure à la force nucléaire (cohésion), c’est le cas lorsque le nombre de protons est supérieur au nombre de nucléons.
Stabilité
On a vu que le noyau est instable si les forces perdent leur équilibre, il y a quelques astuces pour déduire la stabilité d’un noyau. (Attention, il y a des exceptions, mais ces règles s’appliquent au plus grand nombre).
- Pour les atomes dont le nombre de protons est inférieur à 92 (Z < 92), le noyau est stable quand le nombre de neutrons est supérieur au nombre de protons (neutrons > protons) sauf pour H(1) et He(3).
- Le noyau est stable si Z ET N sont pairs. N correspond au nombre de neutrons (N = A – Z). Par exemple 816O.
- Le noyau est stable si Z et/ou N valent 2, 8, 20, 50, 82 ou 126.
Désintégrations radioactives
Les réactions nucléaires impliquent la transformation d’un élément en un autre par modification du noyau. D’après les lois de Soddy (lois de la conservation), il y a conservation du nombre de masse et du nombre de charge. En revanche, les réactions chimiques, impliquent un mouvement d’électrons avec conservation des éléments chimiques.
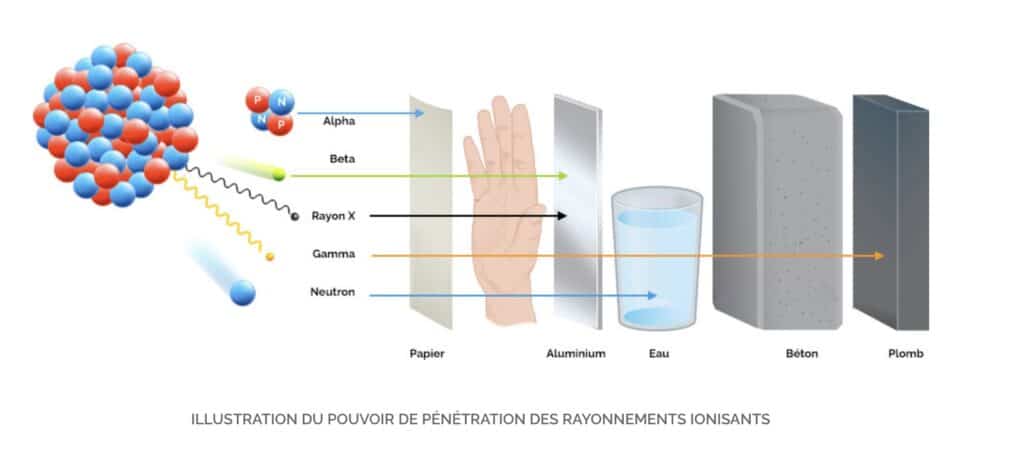
Les noyaux radioactifs se désintègrent spontanément en libérant leur surplus d’énergie et émettent des rayonnements dont le pouvoir de pénétration, la nature ou encore le pouvoir ionisant diffèrent. Les rayons alpha (α) peuvent être stoppés par une simple feuille de papier, les rayons bêta (β) par de l’aluminium et les rayons gamma (γ) par du plomb.
Rayonnement α
Il s’agit de l’émission d’un atome d’hélium deux fois ionisé (He2+) appelé hélion, c’est la particule alpha. En émettant un atome d’hélium deux fois ionisé, le noyau parent X perd 4 à son nombre de masse (A) et 2 à son numéro atomique (Z), pour donner un noyau fils Y qui n’appartient pas au même élément chimique que celui du noyau X. Ce type d’émission concerne les isotopes lourds (A > 150).
Ainsi, la formule est :
AzX -> A-4z-2Y + 42He
Par exemple l’uranium se transforme en thorium 234 lorsqu’il subit une désintégration alpha :
23892U -> 23490Th + 42He
Les rayonnements alpha sont arrêtés par une feuille de papier ou par la peau donc il ne constituent pas une source de danger externe. Cependant, s’ils sont inhalés ou ingérés ils peuvent être très dangereux en détruisant toutes les cellules autour du fait de leur fort pouvoir d’ionisation. C’est pour cela que ces rayons sont utilisés en médecine de manière très contrôlée pour détruire des cellules cancéreuses, on peut aussi les retrouver dans certains détecteurs de fumée. Mais c’est aussi un phénomène naturel qui se produit dans les roches.
Rayonnements β-
Il s’agit de l’émission d’un électron (e-) et d’un antineutrino (v-). En émettant ces deux particules, le noyau parent X gagne 1 à son numéro atomique (Z) et reste constant dans son nombre de masse, pour donner un noyau fils Y. On peut en déduire qu’il y a eu conversion d’un neutron en proton. Ce type d’émission concerne les noyaux possédant un excès de neutrons.
Ainsi, la formule est :
AzX -> Az+1Y + 0-1e- + 00v-
10n -> 11p + 0-1e- + 00v-
Par exemple :
4019K -> 4020Ca + 0-1e- + 00v-
On retrouve aussi ce type de désintégration dans la nature (corps, pierres volcaniques, bananes) et on peut l’utiliser en médecine nucléaire (PET-scans, traitements)
Rayonnement β+
Il s’agit également d’une transformation isobarique car A reste constant. Cette fois il y a émission d’un positron (e) et d’un neutrino (v). En émettant ces deux particules, le noyau parent X perd 1 à son numéro atomique (Z) et reste constant dans son nombre de masse, pour donner un noyau fils Y. Il y a conversion d’un proton en neutron. Ce type d’émission concerne les noyaux possédant beaucoup de protons.
La formule est :
AzX -> Az-1Y + 0+1e+ + 00v
11p -> 10n + 0+1e+ + 00v
Par exemple :
189F -> 188O + 0+1e+ + 00v
Ce type de désintégration est plus rare dans la nature, on l’utilise surtout avec des isotopes artificiels en médecine nucléaire (imageries métaboliques, PET-scans).
Les rayonnements β (+ et -) sont très dangereux, car ils peuvent faire des dégâts en exposition externe ou interne au corps. Bien qu’ils aient un pouvoir ionisant plus faible que les rayons alpha, ils peuvent brûler la peau ou les yeux et engendrer des mutations de l’ADN qui peuvent causer des cancers.
Rayonnements γ
Après avoir subi des désintégrations α ou β, le noyau se trouve souvent dans un état excité noté X*. L’émission gamma résulte de l’évacuation d’un surplus d’énergie de ce noyau excité sous forme d’un photon de très haute énergie qui correspond à un rayonnement électromagnétique gamma (y).
On note cela :
AZX -> AZX + 00γ
Par exemple le Thorium retombe à son état fondamental en émettant un photon gamma :
23490Th -> 23490Th + γ
Dans ce type de désintégration, A et Z restent constants (l’élément reste le même), car il n’y a pas d’émission de particules. On la retrouve dans la nature (rayonnement cosmique), dans l’industrie (contrôle de soudures, mesures…) ou encore en médecine (scintigraphie, radiothérapie).