Les réactions d’oxydoréduction sont indispensables dans de nombreux domaines, comme la protection contre la corrosion, la synthèse de produits chimiques, la production d’énergie (pile), la respiration cellulaire et bien d’autres ! Il est donc essentiel de comprendre leur fonctionnement en chimie.
Couples REDOX
À chaque couple redox correspond une demi-équation de la forme suivante :
Ox + ne− 
Les conventions veulent que l’oxydant soit du côté gauche (le couple va dans le sens de la réduction).
Il est à noter que les demi-équations ne signifient rien toutes seules, car une réaction redox se produit entre deux couples, de plus dans les demi-équations, les électrons sont toujours du coté de l’oxydant.
Exemples de couples :
- Cl2(g)/Cl– : Cl2(g) + 2e-
2Cl–
- H+/H2 : 2H+ + 2e-
H2(g)
- S4O62-/S2O32- : S4O62- + 2e-
2S2O32-
Oxydation
Une oxydation correspond à une perte d’électrons. Un réducteur est une espèce capable de céder un ou plusieurs électrons.
Pour le couple Fe3+/Fe2+ :
Fe2+ 
Le réducteur est Fe2+ et l’oxydant est Fe3+, il s’agit d’une réaction d’oxydation.
Réduction
Une réduction correspond à un gain d’électrons. Un oxydant est une espèce chimique capable de capter un ou plusieurs électrons.
Pour le couple (I2(S)/2I–)
I2(S) + 2e- 
L’oxydant est I2(S) et le réducteur est 2I–, il s’agit d’une réaction de réduction.
Réactions d’oxydo-réduction
Il s’agit d’une réaction de transfert direct d’électrons entre 2 couples redox.
- Oxydant 1 + n1e-
Réducteur 1 (* n2)
- Réducteur 2
Oxydant 2 + n2e- (*n1)
- n2Oxydant1 + n1Réducteur2
n2Réducteur1 + n1Oxydant2
Application
Soit les couples H+(aq)/H2(g) et Na+(aq)/Na(s)
- Réaction de réduction : 2H+(aq) + 2e–
H2(g)
- Réaction d’oxydation : (Na(s)
Na+(aq) + 1e-)*2
On multiplie par 2 cette réaction d’oxydation car les électrons formés doivent être utilisés en totalité lors de la réduction de H+. Il n’y a jamais d’e- libres en solution.
- Réaction bilan : 2Na(s) + 2H+(aq)
2Na+(aq) + H2(g)
Potentiel standard
Dans la réaction précédente entre H+/H2 et Na+/Na, comment sait-on quel couple se réduit et quel couple s’oxyde ? On peut utiliser le potentiel standard E° des couples.
Par convention, un potentiel est défini pour chaque couple dans le sens de la réduction de sa demi-équation (Ox + ne- 
Sa formule est : 2H+(aq) + 2e- 
C’est le potentiel 0 de l’hydrogène.
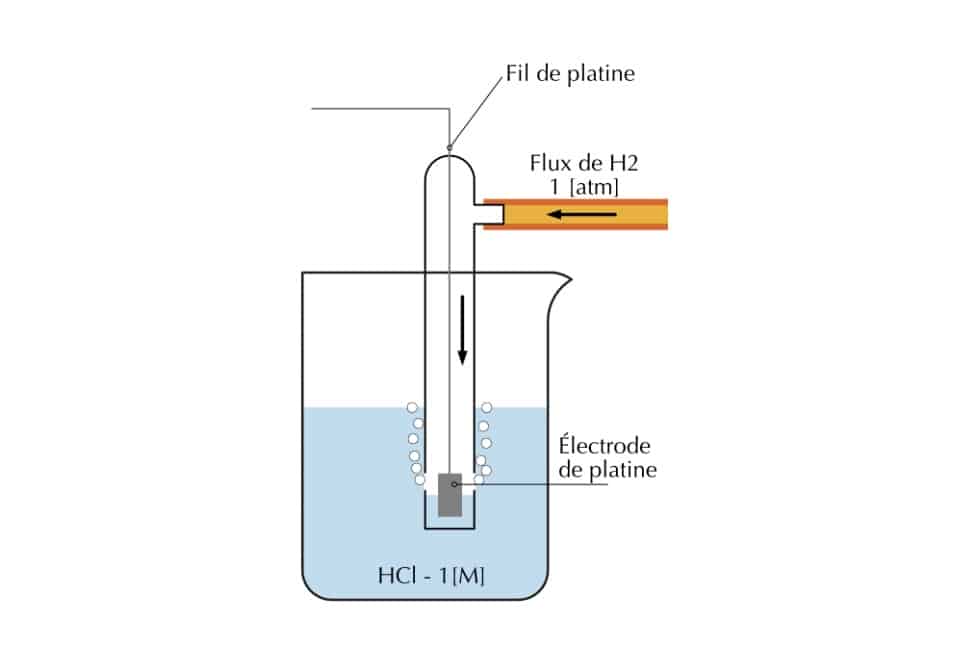
En pratique, on utilisera plutôt une autre électrode de référence : L’électrode au calomel saturé (ECS).
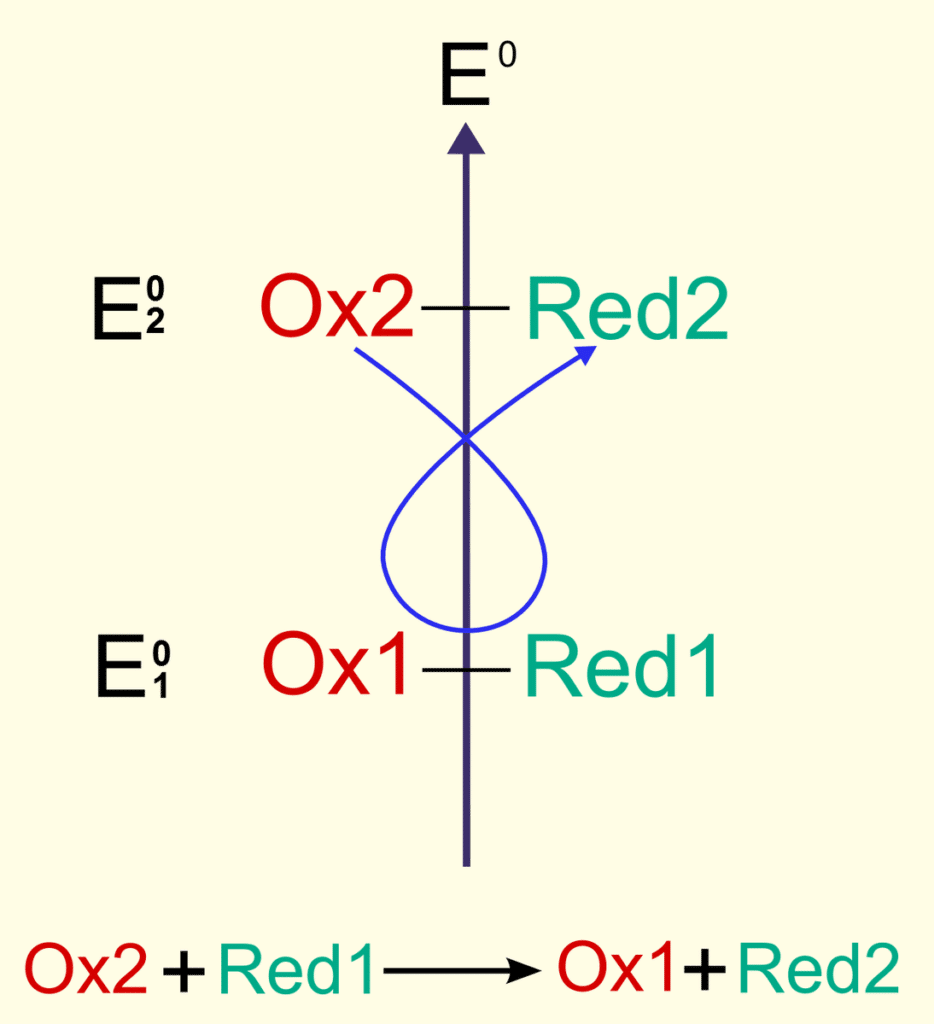
Plus E° est élevé, plus l’oxydant est fort et plus le réducteur conjugué est faible. Plus E° est faible, plus le réducteur est fort, plus l’oxydant conjugué est faible.
Quand il y a deux couples présents, la réaction va se réaliser spontanément dans un seul sens, c’est le critère de spontanéité. La réaction se produit spontanément si l’oxydant est celui du couple avec le potentiel redox le plus élevé avec le réducteur du couple avec le potentiel redox le plus bas. (L’oxydant le plus fort réagit avec le réducteur le plus fort). La technique est la suivante :
La pile
Pile Daniell
Une des applications les plus courantes de l’oxydoréduction est la pile, qu’on modélise souvent en travaux pratiques par la pile Daniell.
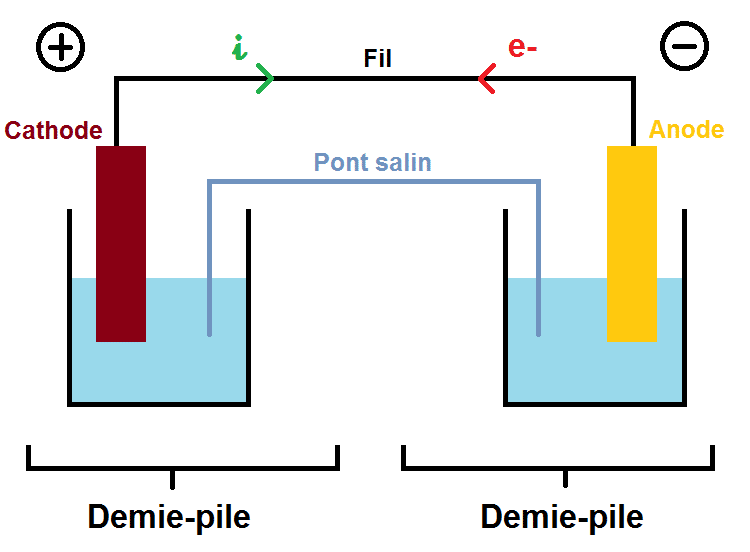
Cette pile est composée de deux électrodes immergées chacune dans une solution d’électrolytes formant une demie-pile. Les électrodes sont reliées par un fil électrique conducteur. Un pont salin relie les deux solutions afin d’assurer l’électroneutralité des solutions en compensant la migration des électrons par des ions et de créer un vrai circuit fermé.
- L’anode est le siège de l’oxydation, elle est toujours négative dans le cas d’une pile, l’électrode de Zn métallique est plongée dans une solution de Zn2+ et NO3–. Couple redox : Zn2+/Zn. Équation à l’anode : Zn(s) -> Zn2+(aq) + 2e-.
- La cathode est le siège de la réduction, elle est toujours positive dans le cas d’une pile, l’électrode de Cu métallique est plongée dans une solution de Cu2+ et NO3–. Couple redox : Cu2+/Cu. Équation à la cathode : Cu2+(aq) + 2e- -> Cu(s)
- Réaction bilan de la pile : Cu2+(aq) + Zn(s) -> Cu(s) + Zn2+(aq)
Ainsi, on a les électrons qui vont de l’anode à la cathode et le courant qui va de la cathode vers l’anode.
L’épaisseur de la plaque de zinc diminue tandis que l’épaisseur de la plaque de cuivre augmente par dépôt de cuivre.
Le système va évoluer jusqu’à l’équilibre des potentiels dans les deux compartiments. La force électromotrice (fem) est constante et vaut :
- Efem mesurée = Ucathode – Uanode
Loi de Nernst
L’équation de Nernst permet de relier le potentiel d’électrode aux activités des espèces impliquées dans une réaction redox.
- Pour une demi-réaction : aOx1 + ne-
bRed1
- La formule est : E = E°(ox/red) + ((R.T)/(n.F))ln(a(Ox1)a/a(Red1)b)
Avec E le potentiel de l’électrode (en V), E° le potentiel standard d’oxydoréduction à la température T, R la constante des gaz parfaits ( R = 8,314 J/K/mol), T la température (en K), F la constante de Faraday (F = 96 500 C/mol), n le nombre d’électrons échangés et a l’activité de l’espèce considérée.
- Forme simplifiée : E = E°(ox/red) + (0,06/n)log(a(Ox1)a/a(Red1)b)
Avec a d’un solvant = 1, a d’un composé solide ou liquide seul dans sa phase = 1, a d’un gaz parfait = P/P° (avec P° = 1 bar), a d’un soluté = C/C° avec C° = 1,00 mol/L.
Connaître la formule est important, mais s’entraîner l’est encore plus. N’hésite pas à faire quelques exercices.
Moyens mnémotechniques :
- anode et oxydation = voyelles ; cathode et réduction = consonnes
- OIL : Oxydation Is a Loss ; RIG : Reduction Is a Gain